【编者按】
声流体技术正为外泌体研究开辟全新路径。瑞典AcouSort公司凭借其创新芯片技术获得欧洲创新理事会2600万瑞典克朗资助,将联合多所高校与企业共同开发血液外泌体分离方案。这一突破不仅彰显声流体技术在生物医学领域的应用潜力,更预示着外泌体诊断技术即将迎来重要进展。随着EVOGEX等专业平台持续发力,外泌体研究与产业化进程有望按下”加速键”。
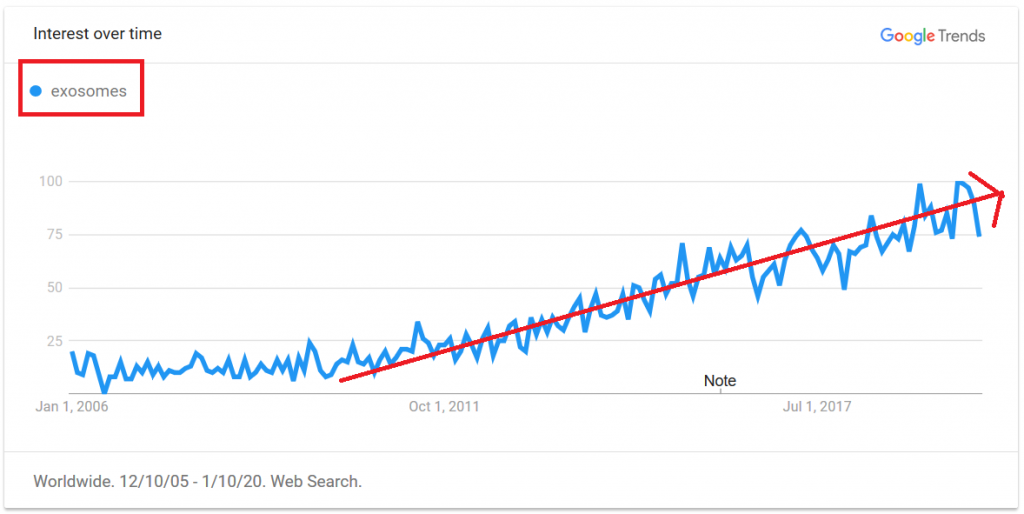
AcouSort AB是一家瑞典公司,率先开发声流体技术,并致力于基于外泌体的诊断研究。2022年8月,欧洲创新理事会(EIC)向AcouSort及其项目合作伙伴授予2600万瑞典克朗(约合250万美元),用于开发从血液中分离外泌体的声流体薄膜驱动芯片。其中约一半资金将直接拨给AcouSort,其余资金则提供给AcouSort的合作伙伴隆德大学、丹麦技术大学和Day One公司。
EVOGEX是Evora公司的专有治疗发现平台,利用工程化外泌体。EVOGEX的目的是增强外泌体的关键特性,并提高基于外泌体的治疗方法的疗效。Evora基于CNRS和巴黎大学实验室在共聚物凝胶和外泌体方面的世界级研究,正在开发其EVOGEX-Digest。其主要产品EVOGEX-Digest旨在显著改善几种胃肠道相关适应症的患者预后。
TheraXyte BioScience是一家专注于细胞外囊泡(EV)介导的药物递送和基于EV的新型疗法的生物技术公司。该公司开发了一个基于EV的药物递送平台(TAXY™),可以在GMP生产水平上大规模生产可修饰的EV。该平台旨在促进有效载荷包装,从而帮助靶向感兴趣的器官/细胞,在这些部位释放有效载荷药物分子和活性生物分子作为治疗方法。
外泌体是大小在30-100纳米之间的小囊泡,存在于几乎所有真核生物体液中,促进一系列重要的细胞功能。它们将DNA、RNA和蛋白质转移到其他细胞,从而改变目标细胞的功能。

目前已有至少26,805篇关于外泌体的科学文章发表,301项临床试验正在进行中,这些小型囊泡在一系列治疗应用中具有引人入胜的潜力。
尽管活动频繁,外泌体正受到越来越多的审查,美国FDA于2019年12月6日发布的外泌体产品公共安全通知指出:

目前,尚无FDA批准的外泌体产品。
如今,越来越多的公司正在开发基于外泌体的产品。以下列表展示了全球所有已知正在开发外泌体疗法或诊断产品的公司。
Aegle Therapeutics Corp.是一家首创的、准备进入1/2a期临床试验的生物技术公司,从异体骨髓来源的间充质干细胞(BM-MSCs)中分离细胞外囊泡(“EVs”),用于治疗严重的皮肤病,包括烧伤和大疱性表皮松解症(一种罕见的儿科结缔组织疾病),并预防疤痕形成。Aegle的分离工艺允许从骨髓来源的MSCs生产治疗级细胞外囊泡。2018年4月,美国食品药品监督管理局(FDA)批准了该公司的首个研究性新药(IND)申请,开始在烧伤患者中进行临床试验。