【编者按】
当AI从追求图像美观转向诊断精准,医疗影像技术正迎来关键转折。本期聚焦人工智能在医学影像领域的深度变革:从生成式AI破解罕见病数据困局,到自监督学习降低标注依赖,技术演进始终围绕临床价值展开。这不仅关乎算法优化,更是对生命责任的重新校准——在风险与信任并存的医疗场景中,让AI真正成为医生可靠的“数字战友”,共同守护患者健康。

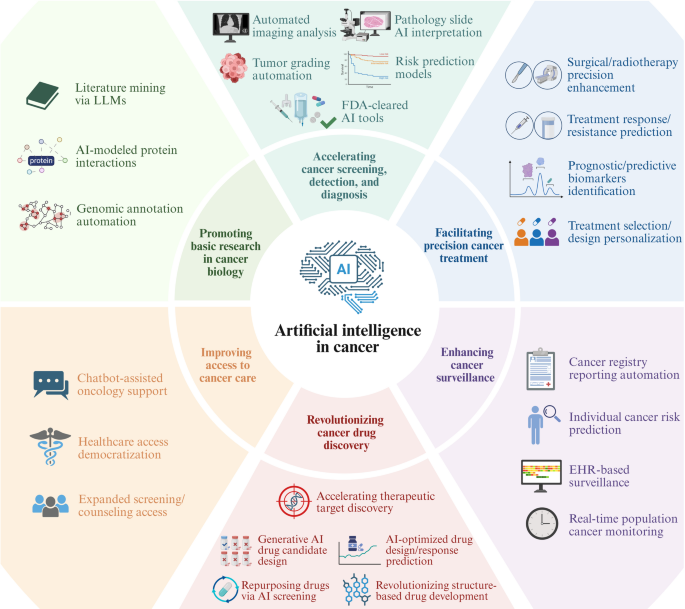
在医疗保健人工智能的关键转变中,研究人员和开发者越来越关注处理医学影像的AI方法的可靠性和诊断准确性,果断超越单纯的美学质量。这种重新优先级的调整凸显了对AI在临床环境中关键作用的成熟理解,在这种环境中,风险天然很高,对技术的信任至关重要。这一关注点的直接意义是推动AI解决方案提供真正可信且具有临床意义的见解,能够增强人类专业知识并改善患者预后。
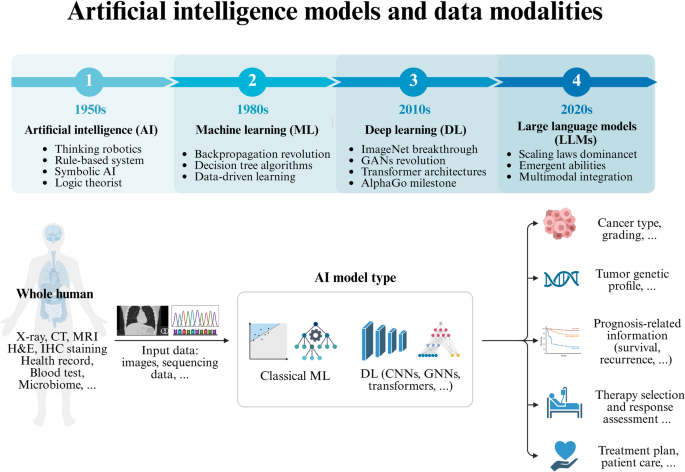
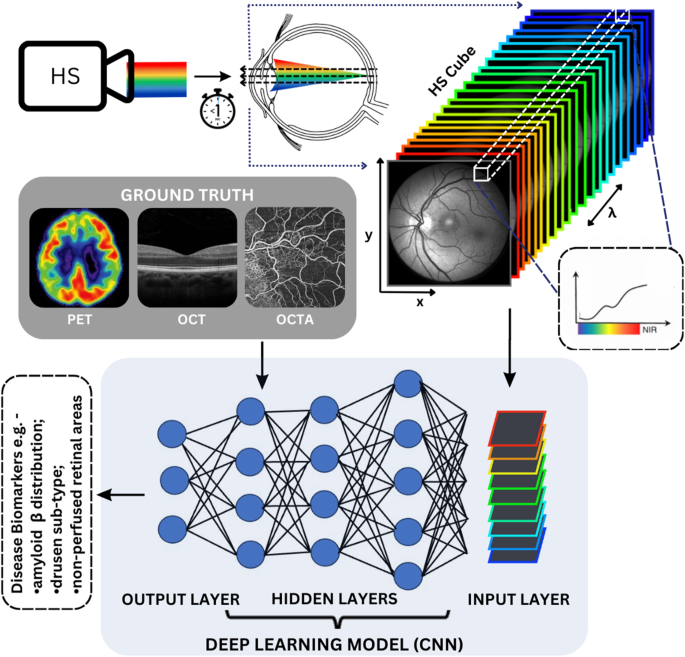
医学影像AI的演进以几项复杂的技术进步为标志,旨在增强诊断效用、可解释性和鲁棒性。生成式AI(GAI)利用生成对抗网络(GANs)和扩散模型等模型,现在不仅用于图像增强,更重要的是用于数据增强,创建合成医学图像以解决罕见疾病的数据稀缺问题。这使得训练更鲁棒的AI模型成为可能,甚至支持多模态转换,例如将MRI数据转换为CT格式以进行更安全的放射治疗规划。这些方法与先前可能优先考虑视觉愉悦结果的方法显著不同,因为新的焦点是从低质量图像中提取细微的病理信号,以改善诊断和患者安全。
自监督学习(SSL)和对比学习(CL)也日益受到关注,减少了对成本高昂且耗时的手动标注数据集的严重依赖。SSL模型在大量未标注的医学图像上进行预训练,学习强大的特征表示,显著提高了肺结节和乳腺癌检测等任务的分类器准确性和鲁棒性。这种方法促进了跨不同成像模式的更好泛化,暗示了医学影像”基础模型”的出现。此外,联邦学习(FL)提供了一种保护隐私的解决方案,以克服数据孤岛问题,允许多个机构协作训练AI模型而无需直接共享敏感患者数据,解决了一个重大的伦理和实践障碍。
UQ方法量化了AI对其预测的信心,对于识别模型可能不太可靠的情况至关重要,从而提示人类专家审查。AI研究界和行业专家对AI革新诊断潜力的初步反应普遍热情,研究表明AI辅助的放射科医生可以更准确并减少诊断错误。然而,存在谨慎的乐观态度,强烈强调严格验证、解决数据偏见以及AI需要作为人类专家的助手而非替代品。
对可靠性、准确性、可解释性和隐私的强化关注正在从根本上重塑医学影像领域AI公司、科技巨头和初创企业的竞争格局。主要参与者如微软(NASDAQ: MSFT)、英伟达公司(NASDAQ: NVDA)和谷歌(NASDAQ: GOOGL)正在大力投资研发,利用其云基础设施和AI能力开发鲁棒的医学影像套件。西门子医疗(ETR: SHL)、GE医疗(NASDAQ: GEHC)和飞利浦(AMS: PHIA)等公司正将AI直接嵌入其影像硬件和软件中,增强扫描仪能力并简化工作流程。
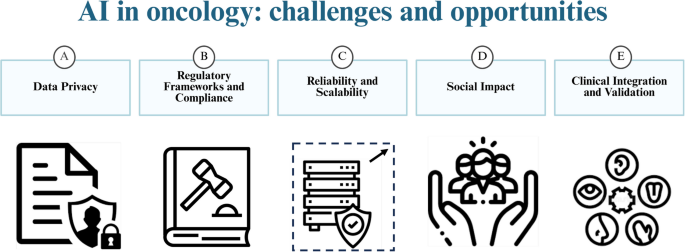
像Aidoc、Enlitic、Lunit和Qure.ai这样的专业AI公司和初创企业,通过为特定诊断挑战提供专注、高准确性的解决方案,正在占据重要的市场地位,通常在紧急病例优先排序或特定疾病检测等领域表现出卓越性能。不断演变的监管环境,特别是即将出台的欧盟AI法案将医疗AI归类为”高风险”,意味着能够明确证明可信度的公司将获得显著的竞争优势。这种严格性虽然可能减缓市场进入,但对于患者和专业信任至关重要,并作为一个强大的差异化因素。
这也意味着对传统工作流程的颠覆,因为AI自动化了常规任务,减少了报告周转时间,并增强了诊断能力。放射科医生的角色正在演变,将他们的焦点转向更高层次的认知任务和患者互动,而不是被取代。采用”人在回路”方法的公司,即AI增强人类能力,在临床环境中更有可能取得成功和被采纳。